La estructura de lewis es una forma de representar los electrones de valencia de un átomo, es decir aquellos electrones que se encuentran en el último nivel energético de un átomo.
Para ello es necesario conocer el número atómico del elemento
y luego determinar la configuración electrónica.
desde allí ubicar los electrones del último nivel.
Para hacer la estructura de lewis de un átomo debes :
1º.- conocer su número atómico (Z).
2º.- hacer su configuración electrónica.
3º.- desde allí sabrás los electrones del último nivel de energía.
4º.- ubicar los electrones alrededor del símbolo del elemento de acuerdo al siguiente esquema.
¿Como es la estructura de lewis del elemento nitrógeno? (Z= 7)
1º.- del número atómico (Z), podemos deducir que el número de electrones del nitrógeno es 7. (átomo neutro) .
2º.- su configuración electrónica es : 1s2-2s2-2p3.
3º.- podemos ver que en el segundo nivel de energía existen 5 electrones(2s2-2p3).
4º.- entonces siguiendo el esquema de lewis podemos escribir .
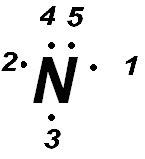 , con lo que la estructura de lewis quedará así
, con lo que la estructura de lewis quedará así
He ahí la estructura de lewis.
Prueba ahora tu solo con la estructura de (Magnesio Mg, Z= 12).
(Fluor Z= 9),
todos los átomos tienden a tener ocho electrones en su último nivel( según la llamada regla del octeto)
como puedes ver el silicio se encuentra estable debido aque en su último nivel de energía posee ocho electrones.
al igual que un gas noble.
Escribe las estructuras de Lewis de los siguientes compuestos, e indica qué átomos presentan cargas formales en los compuestos que sea necesario:

Solución 2.1
| | | |
| | | |
| | | |
| | | |
| | | |
| | | |
| | | |
| | | |




15 comentarios:
Me llama la atención la estructura de Lewis del Nitrógeno; a mí me habían dicho que los electrones no pueden estar desapareados en un orbital y ahí hay 3 desapareados y un par :S
Se puede relacionar con la geometria de las moleculas?? podría subir algo de eso
obviamente el nitrógeno tiene 3 electrones desapareados correspondiente a electrones px-py-pz, con ellos puede enlazar a tres atomos distintos para formar por ejemplo compuestos como el amoniaco(NH3).
(los dos electrones apareados corresponden a electrones en el orbital "s")
Anonima
Esta pagina esta bien buena porque me acaba de enseñar muchas cosas en las que todavia tenia dudas. Aqui esta mejor explicado que en colegio. jajaja :)
Joder lo entiendo por aqui y con mi profesora particular no jajajaj tiene narices la cosa
pero no entiendo porque si el nitrogeno tiene z=7 solo se colacan 5 puntitos alrededor
esque solo se dibujan los de la última capa incompleta (capa de valencia)
El orden en el que se colocan los electrones siempre es el mismo?
Tiene Numero atómico 7, ósea 7 protones en el nucleo y 7 electrones girando al rededor del nucleo, los electrones giren en orbitas o niveles de energía, como las orbitas de los planetas alrededor del sol, los electrones que giran en la ultima órbita son los electrones de valencia y son los que se indican con puntitos en el diagrama De Lewis; quiere decir que 2 electrones giran en la orbita mas cercana al núcleo y solo 5 en la segunda y última orbita del nitrógeno, y como lo que importa en los enlaces son los electrones de la ultima orbita solo se dibujan los 5. Espero sea de ayuda.
Y como queda la estructura de Lewis para el Alumino, tiene 3 electrones en la última capa (3s2 y 3p1)siguiendo el orden que indicaste para acomodar los puntos en la estructura de Lewis quedarían 3 electrones desapareados sin embargo el subnivel s del nivel 3 esta completo y en el N si estas representando con un par de puntos el par de electrones de 2s ??
muy bueno el articulo :)
este es un blog muy interesante,y como lo explica es muy bueno , pero alguien me diria si este blog tiene tambien ENLACE IONICO?
este es un blog muy interesante,y como lo explica es muy bueno , pero alguien me diria si este blog tiene tambien ENLACE IONICO?
¿se puede hacer diagrama de lewis a los del grupo B o es que si se pude?
como se haría la estructura de lewis del elemento cobalto "Co"???????
También quiero saber como quedaría el Cobalto..
Publicar un comentario